Lab № реакции цветни 7 свойства протеин за протеини и аминокиселини
Цвят реакции за протеини Експеримент 1. Реакционната биурет.
Biuret реакция - високо качество за всички, без изключение протеини. и продукти от тяхната частична хидролиза. който съдържа най-малко две пептидни връзки.
Принципът на метода. Биуретът реакция се дължи на присъствието на пептидни връзки в протеини (- СО - NH -), което, в алкална среда, за да се образува меден сулфат (II) боядисани в червено-пурпурен цвят медни соли като комплекси. Биуретът реакция дава някои непротеинови субстанции, като биурет (NH2-CO-NH-CO-NH2), карбоксамид (NH2 CO-CO-NH2), няколко аминокиселини (хистидин. Серин. Треонин. Аспаргин).
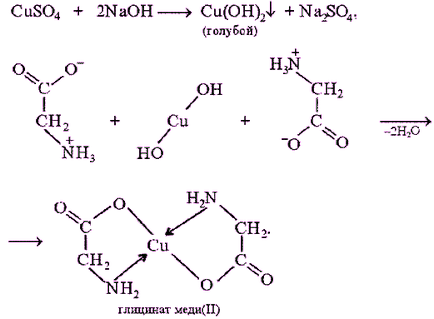
Биуретът реакция с глицин
Редът на изпълнение.
Към 1 мл от разтвор на 1% протеин се прибавя равен обем от 10% разтвор на натриев хидроксид (NaOH) и след това на алкален 2-3 капки на 1% разтвор на меден сулфат (CuSO4). разрежда, почти безцветен разтвор на меден сулфат.
Когато положителна реакция се появява виолетов цвят с червен или син оттенък.
Опитът 2.Reaktsiyana "свободно свързани сяра."
Принципът на метода. Това е реакция на цистеин и цистин. Алкална хидролиза "свободно свързани сяра" в цистеин и цистин доста лесно отцепена, при което се образува сероводород, който реагира с алкални дава натриев или калиев сулфид. Чрез добавяне на оловен ацетат (II), образувана утайка от оловен сулфид (II) сиво-черно.
Редът на изпълнение.
В изсипва тръба 1 мл неразреден пилешки протеин се добавя 2 мл 20% разтвор на натриев хидроксид. Сместа се нагрява внимателно (към сместа се изхвърля).
Това освобождава амоняк, който се разпознава от синка за пране мокро лакмусова хартия, значка за отваряне тръби (не докосват стените). Получената утайка се разтваря при леко кипене под обратен хладник и след това се прибавя 0,5 мл разтвор на оловен ацетат (II). Налице е загуба на сиво-черна утайка оловен сулфид (II):
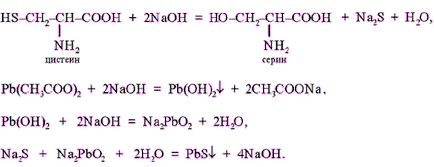
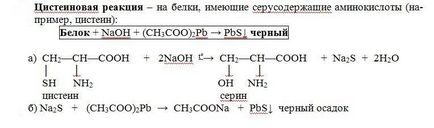
Леярската тръба 1 мл. неразреден пилешки протеин се добавя 2 мл. концентриран алкален разтвор, поставени повече reboilers. Към горещия разтвор се прибавя разтвор на натриев plumbite - образува жълто-кафяв или черен цвят. (Натриев Plyumbit получава както следва: към 1 мл алкален разтвор оловен ацетат се добавя на капки до разтваряне първоначално образуване на утайка от оловен хидроксид).
В присъствието на сяра аминокиселини в молекулата на протеин (цистин, цистеин) на тези аминокиселини се разцепва постепенно сяра под формата на йон в състоянието окисляване - 2, присъствието на която се открива и олово йон, сяра йон образуване неразтворим оловен сулфид, черен:
Pb (CH3 COO) 2 + 2NaOH Pb (ОН) 2 + 2 СН3 COONa,
Pb (ОН) 2 + 2NaOH Na2 PbO2 + Н 2О,
Na2 S + Na2 PbO2 + 2Н2 О PBS + 4NaOH.
Да направим опит: да се направи заключение и пишат на уравнението на реакцията.
3. Опит ksantoproteinovaya протеини отговор.
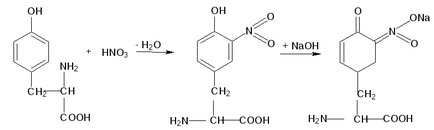
Принципът на метода. Тази реакция се използва за откриване на а-аминокиселини, съдържащи ароматни радикали. Тирозин, триптофан, фенилаланин чрез реакция с концентрирана азотна киселина, за да образуват нитро производни с жълто оцветяване. В алкална среда, тези нитро производни на а-аминокиселини дават соли, боядисани в оранжев цвят. Желатин, например, не съдържа ароматни аминокиселини, не ksantoproteinovaya проба.
Редът на изпълнение.
Към 1 мл 10% яйце се прибавя 0,5 мл концентрирана киселина протеинов разтвор азотна. В резултат на протеин коагулация, бяла утайка или мътност в съдържанието на тръбата. При нагряване на разтвора и утайката е оцветен в ярко жълт цвят. В тази утайка почти напълно разтворен в хидролизата. След охлаждане, 2.1 мл 20% разтвор на натриев хидроксид (до оранжев цвят на разтвора).
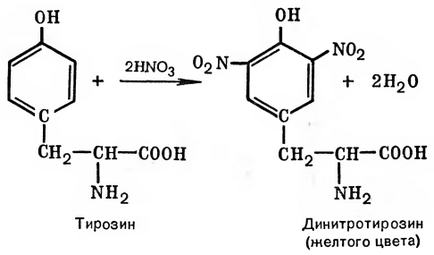
Нека разгледаме механизма на реакцията чрез радикална ksantoproteinovaya тирозин:
Нека разгледаме механизма на реакцията чрез радикална ksantoproteinovaya тирозин:
синьо-виолетов кондензационен продукт
Реакцията с нинхидрин се използва за визуално откриване на а-аминокиселини в хроматограмите (хартия, тънкослойна), а също и за колориметрично определяне на концентрацията на аминокиселини от интензивността на оцветяване на реакционния продукт.
Продуктът от тази реакция съдържа в състава си радикал (R) на първоначалната аминокиселина, което води до различни цвята: синьо, червено и т.н. съединения, произтичащи от реакциите на аминокиселини с нинхидрин.
Понастоящем нинхидрин реакция е широко използван за откриване на отделни аминокиселини, и за определяне на техния размер.
Редът на изпълнение.
Леярската тръба 1 мл от 1,10% сила разреден разтвор на пилешки яйчен белтък и 2,1 мл 1% разтвор на нинхидрин в ацетон. Съдържанието на епруветката и се разбърква в продължение на 2-3 минути внимателно се нагрява на водна баня, докато цвета на синьо-виолетов, което показва присъствието на а-аминокиселини в протеина.
Да направим опит: да се направи заключение и пишат на уравнението на реакцията.
6. Опитът Sakaguchi реакция.
Принципът на метода. Тази реакция на аминокиселината аргинин се основава на взаимодействието на аргинин с а-нафтол в присъствието на окислител. Неговият механизъм все още не е напълно изяснен. Очевидно е, че реакцията се извършва съгласно следното уравнение:
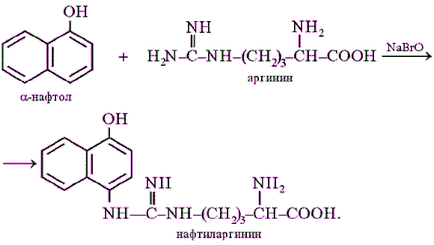
Тъй quinoneimine производни (в този случай нафтохинон), в които водородът на имино група -NH- е заместен с алкил или арил радикал, винаги оцветени в жълти и червени цветове, изглежда, че е оранжево-червен цвят на разтвора по време на реакцията, поради появата Sakaguchi а именно naftohinonimina производно. Не е изключено обаче, вероятността за образуване на по-комплексно съединение поради допълнително окисление на останалата NH-групата на остатък аргинин и бензеновия пръстен а-нафтол:
Редът на изпълнение.
Към 2 мл. От 1% разреден разтвор на пилешки яйчен протеин се добавя 2 мл. 10% натриев хидроксид (NaOH) и няколко капки от 0.2% алкохолен разтвор на α-нафтол. Съдържанието на епруветките се смесват добре. След това се излива 0.5 мл. натриев хипобромит (NaBrO) или натриев хипохлорит (натриев хипохлорит - NaOCl), се разбърква. Веднага става ясно, червено, постепенно увеличаване на оцветяване.
Веднага се добавя 1 мл 40% разтвор на карбамид, за да се стабилизира бързо развитие на оранжево-червен цвят.
Този отговор е характерно за съединения, съдържащи остатък на гуанидин
и показва наличието на протеинова молекула, амино киселини, аргинин:
NH = C -NH - (СН2) 3 -СН -СООН