Кислородът и неговата подготовка
ИМОТИ на кислород и метод за производство на
O2 Кислородът е най-разпространеният елемент на Земята. Това е голям брой химични съединения с различни вещества в кора (50% т.), Във връзка с водород във вода (около 86% тегл.) И в свободно състояние във въздуха в смес от основно азот размер на 20,93%. (23,15% тегл.).
Кислородът е важно в икономиката. Той е широко използван в металургията; химическата промишленост; лечение газопламъчно на метали, огън сондиране хард рок, подземната газификация на въглища; в областта на медицината и различни дихателни апарати, например за височинни полети, както и други области.
При нормални условия, кислород газ е безцветен, без мирис и вкус, незапалим, но активно поддържа горенето. При много ниски температури, кислород се втечнява и дори твърдо вещество.
Най-важните физични константи на кислород следното:
Тегло на 1 m 3 при 0 ° С и 760 mm Hg. Чл. в кг
Същото се при 20 ° С и 760 mm Hg. Чл. в кг
Критичната температура в ° С
Критично налягане в кг / м3
Точката на кипене до 760. Чл. в ° С
Тегло на 1 литър течен кислород при -182, 97 ° С и 760 mm Hg. Чл. кг.
Количеството на кислорода газ, получен от 1 литър течност при 20 ° С и 760 mm Hg. Чл. в л
Точката на втечняване при 760 mm Hg. Чл. в ° С
Кислородът е с висока реактивност и образува съединения с всички химични елементи с изключение на редки газ. реакция на кислород с органични съединения имат подчертано екзотермична характер. Така реакцията с мастни сгъстен кислород или са във фино раздробено твърдо вещество, горими материали настъпва моментната им окисляване и спонтанно запалване на топлината, освободена допринася за вещества, които могат да причинят пожар или експлозия. Този имот е особено да се вземе предвид, когато се занимават с кислородни апарати.
Един от най-важните свойства на кислород е неговата способност да образуват широка гама експлозивни смеси с горими газове и пари на запалими течности, което може да доведе до експлозии в присъствието на открит пламък или искри. Експлозиви и въздух се смесват с горивен газ или пара.
Кислородът може да бъде получен чрез: 1) химични методи; 2) чрез електролиза на вода; 3) физически метод от въздуха.
Химични методи, които се състоят в получаване на кислород от различни вещества, неефективни и понастоящем имат само лабораторна стойност.
Електролиза на вода, т.е. разлагане му в компоненти - .. водород и кислород се осъществява в устройства, известни като клетки. След вода, към която се добавя за подобряване на електропроводимостта на натриев хидроксид NaOH, постоянен ток се предава; кислород, събрана на анода и водород - катода. Недостатък на метода е голяма консумация на енергия: 1 m 3 02 (за освен получи 2 m 3 Н 2) се консумира 12-15 кВт. ч. Този метод е рационално в присъствието на евтина електроенергия, както и при получаването на електролитна водород, когато кислород е отпадъчен продукт.
Физическата методът за разделяне на въздуха в компонент от дълбоко охлаждане. Този метод позволява да се получи кислород в почти неограничени количества и има голямо промишлено значение. Електрическа консумация на енергия на 1 м 3 на O2 е 0.4-1.6 кВт. часа, в зависимост от типа на инсталацията.
Производството на кислород от въздуха
Атмосферния въздух е в основата на механична смес от три газове на следния обемно съдържание на: азот - 78,09% кислород - 20,93% аргон - 0,93%. В допълнение, тя съдържа около 0.03% въглероден диоксид и малки количества от редки газове, водород, азотен оксид и други.
Основното предизвикателство за получаване на кислород от въздуха е за разделяне на въздуха в кислород и азот. Произвежда аргон разделяне Между другото, в който -Application методи специално заваряване непрекъснато се увеличават, както и редки газове, които играят важна роля в редица индустрии. Азот има някои приложение при заваряване като защитен газ, в медицината и други области.
Методът се състои в дълбоко охлаждане с въздух с лечение в течно състояние, което при атмосферно налягане може да се постигне в температурния диапазон от -191,8 ° С (начало на втечняване) до -193,7 ° С (край втечняване).
течно разделяне на кислород и азот се извършва чрез използване на разликата в техните точки на кипене, а именно, на кипене. а2 = -182,97 ° С; Tkip.N2 = -195,8 ° С (при 760 mm Hg. V.).
С постепенното изпаряването на флуид в газообразна фаза основно ще премине азот с ниска точка на кипене и поне изолация течност ще бъде обогатена с кислород. Множество повторения на този процес дава възможност да се получи изисква кислород и азот чистота. Такъв метод за разделяне на течности в съставни части се нарича поправка.
За производството на кислород от въздуха, има специализирани предприятия, оборудвани със съоръжения с висока производителност. В допълнение, големи метални компании имат свои собствени кислородни станции.
Ниските температури, необходими за втечняване на въздуха се получават при използване на така наречените охлаждащ цикъл. Следва обобщение на основните хладилни цикли, използвани в съвременните инсталации.
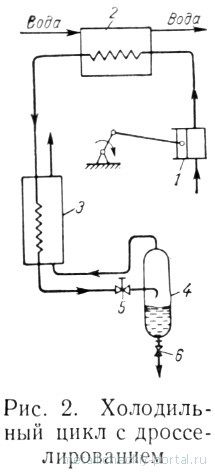
Въздухът се пресова в многостепенен компресор 1 до 200 кгс / см 2 и след това преминава през кондензатора 2 с течаща вода. Дълбоко охлаждане на въздуха се извършва в топлообменник 3, обратен поток от студен газ от течност съд (втечнител) 4. В резултат на разширяване на въздуха в дроселната клапа 5, се охлажда и частично втечнен.
Налягане при събирането 4 се контролира в обхвата от 1-2 кгс / см 2. течност периодично се оттича от колекция в специални контейнери през вентил 6. Neszhizhennaya част на изпуска през топлообменника въздуха, създавайки нови охлаждащи части на входящия въздух.
въздушно охлаждане до температура на втечняване е постепенно; при определянето е сменил началния период, през който не се наблюдава въздушния втечняването, но само охлаждане инсталация се случи. Този период отнема няколко часа.
Едно от предимствата на цикъла е неговата простота, но недостатъкът - сравнително висока консумация на енергия - до 4,1 киловата ч на 1 кг втечнен въздух в компресора при налягане от 200 кгс / см 2; при по-ниско налягане потребление относителна мощност се увеличава драстично. Този цикъл се използва в системи за ниско и средно капацитет за производство на газообразен кислород.
Малко по-сложно е цикъл с дроселиращ и предварително въздушно охлаждане амоняк.
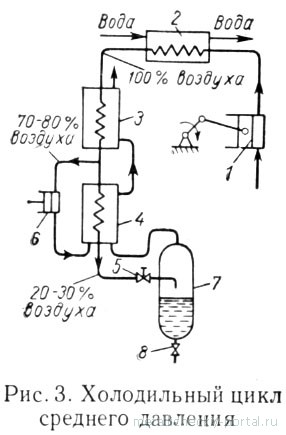
Въздухът се пресова в компресора 1 и 20-40 кгс / см 2 преминава през охладителя 2 и след това през топлообменници 3 и 4. Когато топлообменника 3, повечето от въздуха (70-80%) се ръководи в буталото за разширение машина разширител 6 и долната част въздух (20-30%) е свободен разширяване на разширяване клапан 5 и допълнително колектор 7 с клапан 8 за източване на течността. Разширителя 6
въздух, вече охлажда в първия топлообменник, произвежда работа - избутва буталото машина, налягането пада до 1 кгс / см 2, при което температурата пада рязко. Разширител студен въздух с температура от около -100 ° С, разредена навън през топлообменниците 3 и 4, охлаждане на входящия въздух. Така разширителя осигурява много ефективен монтаж охлаждане при относително ниско налягане на компресора. Работният разширителя се използва и е полезно да се компенсира частично за разходите на енергия за въздух компресия в компресора.
Предимствата на цикъла са относително малък натиск компресия, което опростява конструкцията на компресора и повишен капацитет на охлаждане (чрез разширител), който осигурява стабилна работа на устройството при избора на кислород в течна форма.
Цикълът на охлаждане с разширение при ниско налягане в турборазширител проектиран Acad. P. L. Kapitsey, въз основа на прилагане на ниско налягане студен въздух за да се получи само поради разширение на въздуха във въздуха турбина (турбина разширяване) на с производство на външната работа. Управление цикъл е показан на фиг. 4.
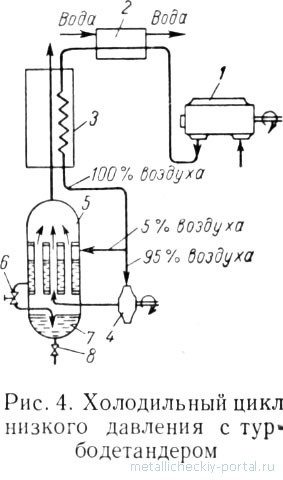
Въздухът сгъстен от турбокомпресора 1 до 6,7 кгс / см 2 се вода охлажда в хладилник 2 и 3 влиза регенераторите (топлообменници), където се охлажда връщане потока студен въздух. До 95% от въздуха след регенераторите се изпраща към турбината за разширение 4 се разширява до налягане 1 кгс / см 2 с изпълнението на външната работа и по този начин се прекъсва, след което се подава в тръба пространство на кондензатора 5 и кондензира останалата част от сгъстения въздух (5%) които влизат в пръстена. От кондензатора 5 на основния въздушен поток към регенератора и охлажда входящия въздух, течност и въздух преминава през дроселната клапа 6 в колектора 7, от която се отделя чрез клапан 8. Диаграмата показва един регенератор, а в действителност те дават малко и включва последователно.
Предимствата на цикъла ниско турборазширител налягане е по-високо, на ефективността на turbomachines сравнение с бутален тип машини, опростяване на технологичната схема, увеличаване на надеждността и взривозащитени инсталация .... Цикълът се използва в инсталацията на голям капацитет.
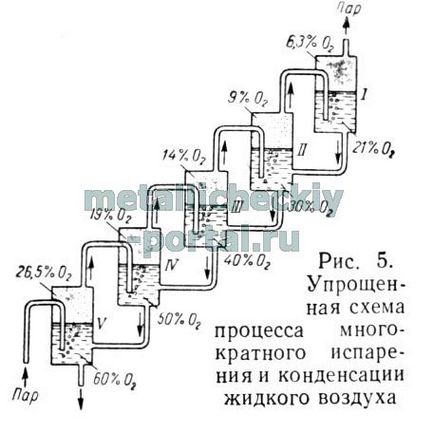
Естеството на процеса на отстраняване може да доведе показано на фиг. 5, опростена диаграма на процес на повторно изпаряване и кондензация на течен въздух.
Да предположим, че в съд II е течност, съдържаща 30% от съда 02. III - 40%, в съд IV - 50%, в съд V - 60% кислород.
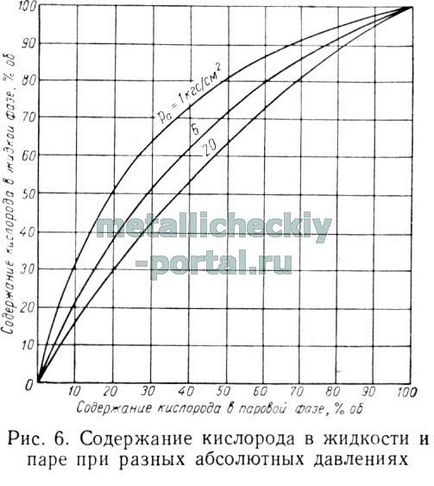
Започнете да се изпари течността в съд V при абсолютно налягане от 1 кгс / см 2. Както се вижда от фиг. 6, над течността в съда, състоящ се от 60% 02 и 40% N2. То може да бъде в състава от равновесното парно съдържащ 02 до 26,5% и 73,5% N2. като същата температура като течността. Снабдяване на парата в съд IV, където течността съдържа само 50% от 02% N2 и 50 и следователно ще бъде студено. Фиг. 6 че двойките тази течност може да съдържа само 19% от 02 и 81% N2. и само в този случай температурата се равнява температура на течността в този съд.
Следователно, предоставена в съда от съд V IV пара, съдържаща 26.5% О2. Той има по-висока температура от течността в съд IV; Следователно кислород пара се кондензира в съд IV флуид, и част от азота, ще се изпари от нея. В резултат на това течността в съд IV обогатен с кислород и пара над него - азот.
По същия начин, процесът ще се появят в други съдове и по този начин, когато източване на горния съд в долната течността обогатен с кислород чрез кондензиране от повишаването на парата и като им на азот.
Независимо от технологичната схема и вида на монтаж на процеса на цикъл замразяване за получаване на кислород от въздуха, съдържащ етапите на:
1) за почистване на въздуха от прах, водна пара и въглероден диоксид. Свързването на СО2 се постига чрез пропускане на въздух през воден разтвор на NaOH;
2) пресоване на въздуха в компресор, последвано от охлаждане в хладилник;
3) охлаждане на сгъстения въздух в топлообменниците;
4) разширяване на сгъстен въздух към вентила за разширение или разширител за неговото охлаждане и втечняване;
5) втечняване и отстраняване на въздух за получаване на кислород и азот;
6) източване на резервоара за течен кислород и неподвижна газоразрядни в резервоари газове;
7) Контролът на качеството на получения кислород;
8) напълване течен кислород, резервоари и транспортни контейнери, напълнени с газообразен кислород.
Качество на газообразен и течен кислород се регулират съответните гости.
Използва се за интензификация на различни процеси в металургията, химическата промишленост и други технологични кислородни съдържа 90-98% О2.
Качествен контрол на газообразен и течен кислород и се прави директно по време на производството с помощта на специални устройства.