Методи за промяна на вътрешния енергиен
Вътрешна енергия може да се променя по два начина.
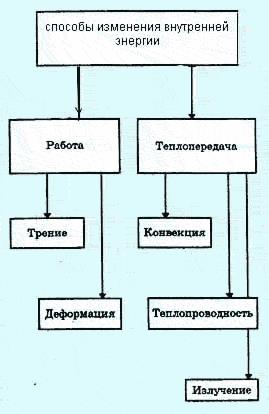
Ако работата се извършва на тялото, вътрешните си енергийни увеличава.
Вътрешният енергията на тялото (посочени като Е или U) - е сумата на енергиите на молекулните взаимодействия и термични движения на молекули. Вътрешната енергия е уникална функция на състоянието на системата. Това означава, че всеки път, когато системата е в това състояние, вътрешната енергия е на присъщата стойност на тази държава, независимо от историята на системата. Следователно, промяната във вътрешната енергия при прехода от едно състояние в друго винаги ще бъде равен на разликата между стойностите в началните и крайните си състояния, независимо от пътя, който прави прехода.
На вътрешната енергия на тялото не може да се измерва директно. Трябва само да се определи промяната в вътрешна енергия:
- - обобщи на топлината на тялото, измерена в джаули
- [1] - работата, извършена от тялото срещу външни сили, измерена в джаули
Тази формула е математически израз на първия закон на термодинамиката
За Квазистатично процеси следната зависимост:
- температура, измерена в градуси по Келвин
- ентропия, измерена в джаули / Келвин
- налягане, измерено в паскали
- броят на частици в системата
Топлината на изгаряне на горивото. Конвенционални гориво. Количеството на въздуха, необходим за горене на гориво.
На гориво се съди по своята калоричност. За характеризиране на твърди и течни горива е специфичната топлина на индекс горене, който представлява количеството на топлината, генерирана от пълното изгаряне на единица маса (кДж / кг). За газообразни горива, скоростта на горене се използва обем топлина, която е количеството на топлината, генерирана от изгаряне на единица обем (кДж / m3). В допълнение, газообразно гориво е в някои случаи оценени от броя на топлината, генерирана от пълното изгаряне на един мол от газ (кДж / мол).
Топлината на изгаряне се определя не само теоретично, но и експериментално, известна част от изгарянето на гориво в специални устройства, наречени топломери. Топлината на горене се оценява чрез повишаване на температурата на водата в колориметъра. Получените по този метод, резултатите е близо до изчислените стойности от елементарния състав на гориво.
Q 14Izmenenie вътрешната енергия чрез нагряване и охлаждане. Работа газ при промяна на силата на звука.
Вътрешният енергията на тялото зависи от средната кинетичната енергия на молекулите и тази енергия се, от своя страна, зависи от температурата. Следователно, промяна на температурата на тялото, и промени вътрешната си тяло отопление energiyu.Pri вътрешната си енергия се увеличава чрез охлаждане се намалява.
На вътрешната енергия на тялото може да се промени без да се извършва работа. Например, тя може да се увеличи, нагревателната плоча на чайника с вода или пропускане на лъжицата в чаша горещ чай. Отоплението е с камина, където жарава, покрив на къщата, осветен от слънцето, и така нататък. Г. при повишаване на температурата на телата във всички тези случаи представлява увеличение с вътрешна енергия, но това увеличение е без работа.
Промяната във вътрешната енергия на тялото, без работа, се нарича пренос на топлина. Топлообмен между телата (или части от същия орган) с различна температура.
Като такива, пренос на топлина се осъществява чрез контакт на студена лъжица с топла вода? Първо, средната скорост и кинетичната енергия на молекулите на гореща вода надхвърля средната скорост и кинетичната енергия на металните частици, от които е лъжица. Но в тези места, където лъжицата е в контакт с вода, топла вода молекули започват да прехвърлят част от тяхната кинетична енергия на лъжиците на частици, и те започват да се движат по-бързо. Кинетичната енергия на водните молекули се намалява и кинетичната енергия на частиците увеличава лъжици. Заедно с промени на енергийните и температура: вода постепенно се охлажда и се нагрява лъжица. Промяна на тяхната температура се провежда в продължение на толкова дълго, колкото и водата, и лъжицата няма да бъде същото.
Част от вътрешната енергия, предавана от едно тяло на друго по време на пренос на топлина, означен със nazyvayutkolichestvom писмо и топлина.
Q - количество топлина.
Количеството топлина, не трябва да се бърка с температурата. Температурата се измерва в градуси, и количеството топлина (както и всяка друга енергия) - в джаула.
При контакт с органи с различна температура по-горещо тяло изпраща определено количество топлина и при най-студен става тялото.
Работа при изобарно разширяване на газа. Един от основните термодинамични процеси, протичащи в по-голямата част от топлинните машини, процеса на разширяване на газа с работа. Лесно е да се определи направено по време изобарен разширяване газ работата.
Когато се появи изобарно разширяването на газа от V1 на обем към обем V2 бутало се движи в цилиндъра на разстояние L (фиг. 106), работната А ', перфектно газ, е
където р - газ под налягане - промени в обема.
Операция на произволна разширяване технологичен газ. Произволното процес на разширяване на газа на V1 на обем към обем V2 може да бъде представена като набор от изобарни и изохорен процеси редуващи.
Работа по време на изотермични разширяване на газа. Сравняване на площи с порции от формите изотермата и isobars, може да се заключи, че разширяването на газа от V1 на обем към обем V2 в същото първоначалната стойност на налягането на газа в случая е придружено от комисия изобарно разширяване повече работа.
Работа компресия газ. Когато разширяване посока газ вектор на силата на налягането на газа съвпада с посоката на вектора на преместване, така че работната А ', перфектно газ е положителен (А'> 0) и работата отрицателен външни сили: А = -А ' <0.
Когато компресиран газ посока вектор на външната сила съвпада с посоката на движение, така че работата позитивна външни сили (А> 0), а работят ", идеален газ, отрицателен (A ' <0).
Адиабатно процес. Освен изобарни, изохорен и изотермични процеси, термодинамиката често считат адиабатни процеси.
Адиабатен процес е процес, който се случва в термодинамична система в отсъствието на топлообмен с околните структури, т.е.. Е. при условие, Q = 0.
Въпрос 15 Условия за равновесие на тялото. Момент на сила. Видове равновесие.
Баланс, или баланс, определен брой свързани с тях явления в областта на естествените и хуманитарните науки.
Системата се счита, че е в равновесие, ако всичко в системата, се компенсира с други ефекти, или не съществува. Подобна концепция - стабилност. Равновесието може да бъде стабилна, нестабилна или безразлични.
Типични примери на равновесие:
1. механична баланс, известен също като статично равновесие - състоянието на тялото в състояние на покой или на движещи се равномерно, в който сумата на сили и моменти, действащи върху него е нула.
2. Химическа равновесие - позиция, в която химическа реакция се извършва в същата степен като обратната реакция, и в резултат не се променя количеството на всеки компонент.
3. физическото равновесие на хора и животни, които се водят от разбирането за необходимостта от него и в някои случаи - с помощта на изкуствено поддържане на този баланс [източник не е посочено 948 дни].
4. термодинамично равновесие - състояние на системата, в която вътрешните процеси не водят до промени в макроскопски параметри (като температура и налягане).
P avenstvo нула алгебричната сума от моментите на силите не означава също, че докато тялото е в покой се изисква. С течение на милиарди години, с постоянен период продължава около оста на въртене на Земята, именно защото алгебричната сума от моментите на силите, които действат на Земята от други органи, е много малък. По същата причина, той продължава да се върти с постоянна честота сук велосипедно колело, и само на външни сили да спрат това въртене.
Видове равновесие. На практика той играе важна роля не само на изпълнението на условията за равновесие на телата, но и качествените характеристики на равновесие, наречен съпротивата. Има три вида на баланс тел: стабилна, нестабилна и безразлични. Равновесието се нарича стабилен, ако след известно влияние на външни фактори тялото се връща в първоначалното си състояние на равновесие. Това се случва, когато леко изместване на тялото във всяка посока от първоначалното положение на резултантната сила действа върху тялото, е различна от нула и е насочено към позиция на равновесие. Стабилната равновесие е, например, една топка на дъното на вдлъбнатината.
Общото състояние на равновесие на тялото. Комбинирането на двата терминала може да бъде формулиран общо състояние тяло баланс: тялото е в равновесие ако геометричната нулев вектор сумата на всички сили, приложена към него и алгебрични сумата от моментите на тези сили около оста на въртене.
Въпрос 16Paroobrazovanie и кондензация. Изпаряване. кипяща течност. Зависимостта на налягането течност кипене.
Изпаряване - имот капчица да се промени тяхното физическо състояние и да се превърне в пара. Изпаряване, което се случва само по повърхността на капчицата се нарича изпаряване. Изпаряване около обема на течност се нарича точка на кипене; това се случва при определена температура, която зависи от налягането. Налягането, при което течността кипи при дадена температура, наречен PNP парно налягане, стойността му зависи от вида на течност и температурата.
Изпаряването - процесът на преход на вещество от течност в газообразно състояние (пара). Процесът на изпаряване е обратен процеса на кондензация (преход от пара за течност изпаряване (изпаряване), преходът от кондензиран вещество (твърдо вещество или течност) в газова фаза (пара). Първо за фазов преход.
Кондензацията - процес обратния процес изпаряване. Когато пари кондензират молекули обратно течност. В затворен съд с течност и пара може да бъде в динамично равновесие, броят на молекули, бягство от течността, равен на броя на молекулите, връщайки се от парата на течност, т.е., когато скоростта на изпарение и кондензационни процеси са идентични. Такава система се нарича двуфазна. Парата в равновесие с течен си, наречена наситен. Броят на молекули бягство течната повърхност на квадратните елементи в секунда, в зависимост от температурата на течността. Броят на молекули, връщайки се от парата към течността зависи от концентрацията на молекулите на пара и средната скорост на тяхната термична движение, което се определя от температурата на парата.
Кипене - процес изпаряване на течността (преход на вещество от течност в газообразно състояние), с появата на граници за разделяне на фазите. Точка на кипене при атмосферно налягане е обикновено като един от основните физикохимични характеристики на химически чиста субстанция.
Вари се отличава от тип:
1. конвекция кипене в голямо количество;
2. вари принудителна конвекция;
3, както и по отношение на средната температура на температурата на течността насищане:
4. Течен кипене subcooled до температура на насищане (вряща повърхност);
5. Температурата на течност кипене до насищане dogretoy
Вари в която пара се получава под формата на мехурчета и нарастващите periodicheskizarozhdayuschihsya наречени кризис кипене. При бавно кризис кипи в течността (или по-скоро, обикновено по стените или на дъното на съда) се появяват мехурчета пълни с пара. Поради силната изпарението на течността вътре в мехурчетата растат те изплуват, и парата се освобождава в парната фаза над течността. В течността в граничния слой е малко прегрята, т.е.. Е. температура му надвишава номиналната точка на кипене. При нормални условия, тази разлика е малка (от порядъка на един градус).
Чрез увеличаване на топлинния поток в определена критична стойност на отделните мехурчета се обединяват, за да образуват непрекъснат контейнер стена в слоя на парата, периодично изригване в течно състояние. Това се нарича провален.